Wärmebehandlung von Stahl (1) 02.09.2010, 11:18
Glühen, Härten und Vergüten sind die wichtigsten Wärmebehandlungsverfahren bei Werkstücken aus Stahl. Die Grundlage für ihr Verständnis sind Gefügeveränderungen beim Erwärmen. Ein wissenschaftliches Thema, das wir durch erlaubte Reduktion verständlich darstellen wollen.
3. und 4. Ausbildungsjahr
Wärmebehandlung von Stahl
1. Grundlagen
Viele Stahlteile in Maschinen und Geräten sind wärmebehandelt. Was versteht man unter »Wärmebehandlung«?
Man wird zuerst an das Gießen und Schmieden denken. Dies sind Verfahren, die den Einsatz großer Wärmemengen erfordern.
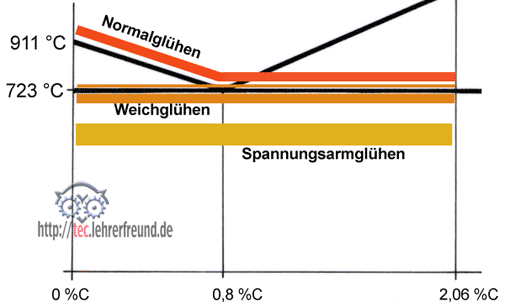
Die hier zu besprechenden Wärmebehandlungsverfahren jedoch haben eine andere Zielsetzung: Man will mit ihnen eine Veränderung und damit eine Verbesserung des Stahlgefüges erreichen; es soll weicher, härter oder zäher werden. Beispiele dafür sind: Nockenwellen, Zahnräder, Ventile (sie alle werden gehärtet), Schrauben, Bolzen, Passfedern (sie werden vergütet); Schweißkonstruktionen werden – wenn ein Verziehen zu befürchten ist - geglüht. Das Glühen, das Härten und Vergüten sind - mit ihren Abwandlungen - die wichtigsten Wärmebehandlungsverfahren.
Zum Verständnis der Wärmebehandlungsverfahren muss man einiges über den Gefügeaufbau wissen. Gemeint ist damit das Innenleben von Metallen.
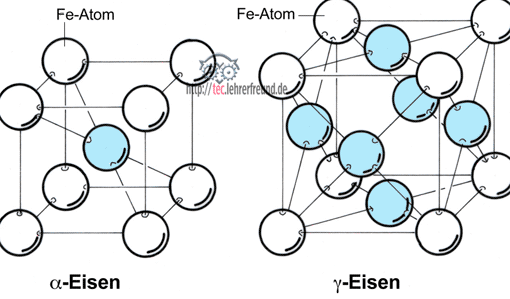
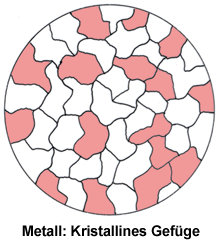
In den Metallen sind die Atome bzw. Moleküle gesetzmäßig, d.h. in Kristallform aneinandergebaut. Beim Erkalten eines flüssigen Metalls entstehen allerdings keine idealen Kristallformen, sondern kristallähnliche Gebilde, die man Kristallite nennt, und die im Querschnitt aussehen können wie im Bild unten dargestellt. Diese Gebilde, die man unter dem Mikroskop sichtbar machen kann, ergeben das Metallgefüge. Kristallin entwickelt sich ein Gefüge deshalb, weil sich die einzelnen Kristalle beim Erstarren des flüssigen Metalls in ihrer Ausformung gegenseitig behindern. Solche Kristallite werden auch als Körner bezeichnet. Von der Korngröße sind wichtige mechanische Eigenschaften des Stahls abhängig; so sind etwa feinkörnige Gefüge zäher und fester als grobkörnige.
2. Beobachtungen beim Erhitzen von Eisen und Stahl
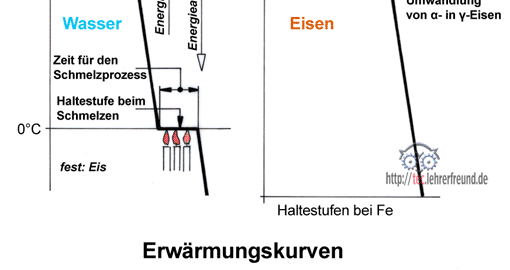
Um die Vorgänge im Stahl, wenn er erhitzt wird, zu verstehen, wollen wir zum Vergleich das Verhalten von Eis und Wasser heranziehen, wenn sie erwärmt werden.
Erwärmt man einen – 5 °C kalten Eisbrocken langsam, dann kann man Folgendes beobachten:
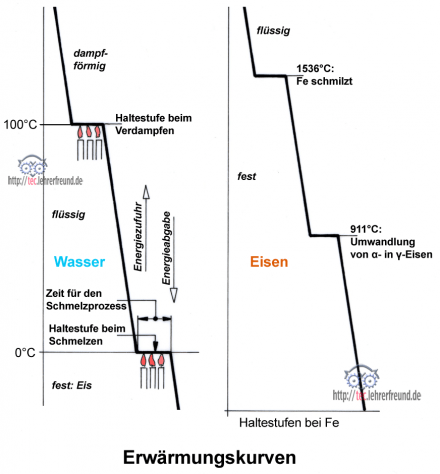
Bei 0 °C beginnt der Eisbrocken zu schmelzen. Es dauert einige Zeit, bis alles Eis geschmolzen ist. Während dieser Zeit bleiben das Eis und das Schmelzwasser trotz konstanter Wärmezufuhr auf 0 °C stehen. Erst wenn alles Eis geschmolzen ist, erwärmt sich das Wasser weiter. Offensichtlich verbraucht Eis von 0 °C also Energie, um zu Wasser von 0 °C zu werden.
Durch weitere Energiezufuhr wird das Wasser nun auf 100 °C erwärmt. Bei dieser Temperatur beginnt das Wasser zu verdampfen. Der entstehende Dampf selbst bleibt so lange 100 °C heiß, bis alles Wasser verdampft ist: Bei weiterer Wärmezufuhr steigt die Dampftemperatur an. Dampfturbinen betreibt man beispielsweise mit bis auf 600 °C überhitztem Dampf.
Zurück zum Versuch: Auch hier bedeutet die »Haltestufe« dies: Um das 100 °C heiße Wasser in 100 °C heißen Dampf umzuwandeln, muss Wärmeenergie zugeführt werden. Oder allgemein: Die Überführung von einem Aggregatzustand in den anderen ist nur mithilfe von Energieeinsatz möglich (fest - flüssig - gasförmig sind die drei Aggregatzustände). Der rechte Pfeil im Bild zeigt: Verläuft der Vorgang umgekehrt, dann wird auf den Haltestufen Energie frei.
Eine ähnliche Beobachtung macht man bei Eisen. Es besitzt zwei für unser Thema wichtige Haltepunkte. Bei 1536 °C geht es vom festen in den flüssigen Zustand über. Unterhalb dieser Temperatur erstarrt das Eisen. Seltsamerweise stellt man bei 911 °C, im festen Zustand also, ebenfalls einen Haltepunkt fest. Bei dieser Temperatur muss demnach, wie wir schon bei der Erhitzung von Wasser sahen, eine Veränderung im Eisengefüge vor sich gehen.
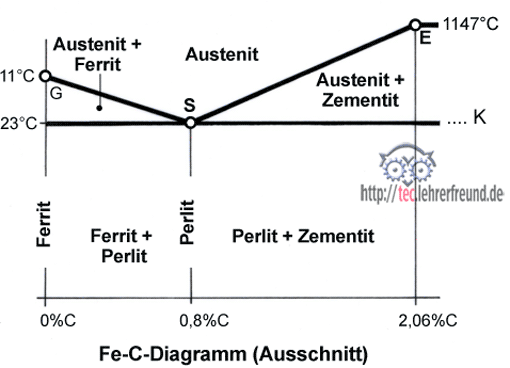
Übrigens: Wenn auch Stahl in der Technik der weitaus wichtigere Werkstoff ist, betrachten wir hier zunächst reines Eisen. Im Stahl, dieser Legierung aus Eisen (Fe) und Kohlenstoff (C), schafft nämlich der Kohlenstoff einige Komplikationen.
____________________________________
Hinweis zur Unterrichtsmethode:
Der Unterricht, der dieses Thema behandelt, kann kein Kreideunterricht sein. Versuche dazu setzen aber einen gut ausgerüsteten Physikraum voraus.
Metallgefüge zeigen: Man benötigt Schliffproben, ein Mikroskop, einen Monitor, der das Schliffbild in ausreichender Größe darstellt. Die Schliffproben sollten praxisnah Stahl- und Graugussproben sein.
Erwärmungskurven:
Eisen erwärmen: Die Temperaturen sind zu hoch, weshalb man auf - wenn es ein Metall sein soll - Zinn (Schmelztemperatur 232 °C) ausweicht. Auch hier gibt es Haltepunkte.
Besser ist es, mit Wasser zu laborieren: Bunsenbrenner, Glasbehälter, Thermometer oder Temperatur-Messsonde, Temperatur-Anzeigegerät, Monitor.
_______________________________
Fortsetzung im Beitrag »Wärmebehandlung von Stahl (2)«