Verbrennungsmotoren: Fahrzeugkatalysator 21.11.2012, 07:50
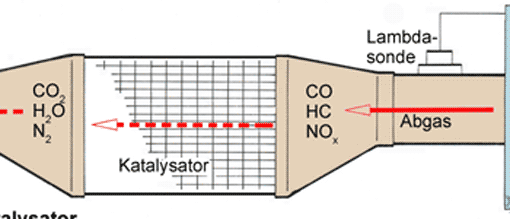
Bei der motorischen Verbrennung entstehen Kohlenwasserstoffe, Kohlenstoffmonoxid und Stickoxide, alle drei giftige Stoffe. Der Katalysator kann die Schadstoffe im Abgas stark reduzieren. So funktioniert er.
Verbrennungsmotoren: Fahrzeugkatalysator
Bei der motorischen Verbrennung entstehen Abgase. Sie enthalten hauptsächlich Kohlenwasserstoffe (CmHn), Kohlenstoffmonoxid (CO), Stickoxide (NOx) und Wasser. Die ersten drei sind für den Menschen und die Umwelt schädlich.
Der Fahrzeugkatalysator, kurz auch Katalysator oder Kat, dient der Nachbehandlung der vom Verbrennungsmotor erzeugten Abgase. Der Kat kann die Schadstoffe stark reduzieren. Als Teil des Auspuffsystems ist der Katalysator in einem Metallgehäuse untergebracht. Seine Aufgabe ist die chemische Umwandlung der Verbrennungsschadstoffe in die ungiftigen Stoffe Wasser (H2O), Kohlenstoffdioxid (CO2) und Stickstoff (N2) durch Oxidation beziehungsweise Reduktion. Bei optimalen Betriebsbedingungen wandelt der Kat die Abgase fast zu 100 % um; so ermöglicht er es, auch strengste Abgasgrenzwerte einzuhalten. Die chemischen Reaktionen haben wir am Ende des Beitrags dargestellt.
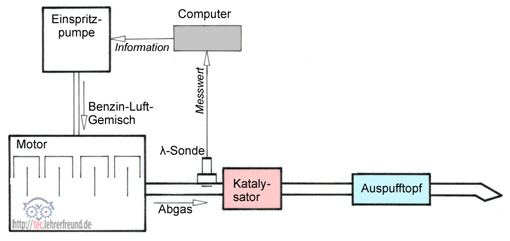
Bei der Nachverbrennung der Abgase wird meistens ein Dreiwege-Katalysator eingesetzt, der die drei genannten Schadstoffe gleichzeitig vermindert.
Der Katalysator besteht aus:
- dem Träger (Keramik- oder Metallträger);
- der Beschichtung (Washcoat) und der Edelmetallauflage, die für die katalytische Wirkung maßgebend ist.
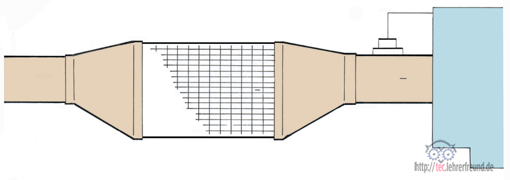
- Die Lambdasonde (λ-Sonde) ist ein Sensor, der im Verbrennungsabgas den jeweiligen Restsauerstoffgehalt misst. Daraus regelt ein Computer das Verhältnis von Verbrennungsluft zu Kraftstoff für die weitere Verbrennung so, dass bei der Verbrennung weder ein Luft-, noch ein Kraftstofftüberschuss auftritt.
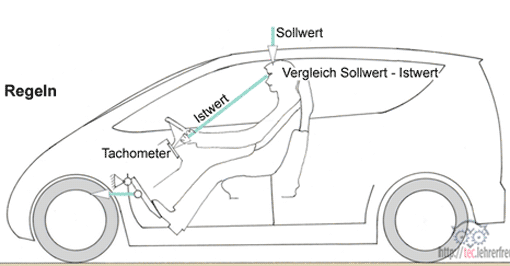
In der Skizze ist ein Regelprozess dargestellt, zu dem es einen separaten Beitrag gibt.
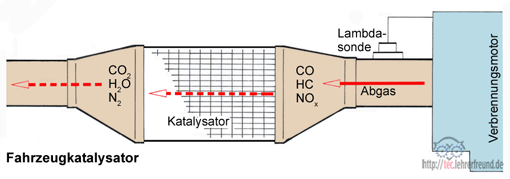
Chemische Reaktionsgleichungen: Im Drei-Wege-Katalysator (auch G-Kat genannt) findet die Oxidation von CO und CmHn sowie die Reduktion von NOx parallel zueinander statt.
Oxidation von CO: 2 CO + O2 => 2 CO2
Oxidation von CmHn: 2 C2H6 + 7 O2 => 4 CO2 + 6 H2O
Reduktion von NO: 2 NO + 2 CO => N2 + 2 CO2
Voraussetzung für die Schadstoffumwandlung ist ein stöchiometrisches Kraftstoffverhältnis (λ = 1) von 14,7 Gramm Luft pro Gramm Superbenzin (Oktan 95) und 14,8 Gramm Luft pro Gramm Normalbenzin (Oktan 91). Bei einer Abweichung zum mageren Bereich (λ > 1) hin steigt die Stickoxidemission nach dem Katalysator sprunghaft an, weil dann der sinkende CO-Anteil für die Reduktion nicht mehr ausreicht. Deshalb wird das Gemisch zwischen stöchiometrischem und leicht fettem Verhältnis geregelt. Der Drei-Wege-Katalysator kann nur bei Fahrzeugen mit Ottomotor und Lambdaregelung eingesetzt werden. Diesel- und Magermix-Ottomotoren benötigen spezielle Katalysatoren.
(Stöchiometrie: Mit ihrer Hilfe werden aus den Teilnehmern einer Reaktion die tatsächlichen Stoffmengen berechnet.)
Ein Hinweis zum Umgang mit chemischen Gleichungen. Der Begriff Gleichung besagt: Links und rechts vom Pfeil stehen dieselben Elemente, und von diesen jeweils dieselbe Anzahl. Beispiel 2 C2H6 + 7 O2 –> 4 CO2 + 6 H2O: Links zählen wir 4 Atome C, 12 Atome H und14 Atome O. Rechts zählen wir: 4 Atome C, 12 Atome H und14 Atome O. (2 C2H6 heißt 2 x das Molekül 2 C2H6). Der Pfeil ist in erster Linie eine Angabe dazu, in welcher Richtung die chemische Reaktion abläuft. Es ist eine Eigenheit der Gase O, H und N, dass sie nur zweiatomig vorkommen, also als O2, H2 und N2.
Die Skizze unten ist für die Verwendung in Aufgabenblättern gedacht.